Katıların Basıncı
Birim yüzeye dik olarak etki eden kuvvete basınç
denir.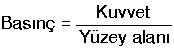
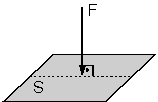
Basınç P, kuvvet F ve yüzey alanı da S ile gösterilirse,
Bu bağıntıya göre, kuvvet sabit ise, basınç yüzey alanı ile ters orantılıdır. Eşit ağırlıktaki tavuğun bataklıkta ördekten daha fazla batmasının nedeni, tavuğun ayaklarının yüzey alanının ördeğinkine göre küçük, dolayısıyla basıncının ördeğinkine göre büyük olmasıdır. Ördeğin ayağı perdeli olduğu için yüzey alanı büyük, basıncı ise küçüktür. Sivri uçlu çivinin ucundaki basınç büyük olduğu için küt uçlu çiviye göre daha kolay çakılır.
Bıçak köreldiği zaman bilelenerek yüzey alanı küçültülür ve basıncın artması sağlanır. Bu nedenle aynı kuvvetle daha kolay kesme işlemi sağlanmış olur.
| Basınç, birim yüzeye etkiyen dik kuvvet idi. Şekildeki cisim yatay ve düşey duvarlar arasındadır. Cismin ağırlığı yatay duvara etki ettiği için yatay duvara basınç uygular. Düşey duvara ağırlığından dolayı kuvvet uygulamadığı için basınç da uygulanmaz. | 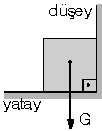 |
| Şekildeki cisim belirtilen yer-den düşey olarak kesilirse, her bir parçanın basıncı bütün cismin basıncına eşit olur. | 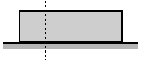 |
Katılar kendilerine uygulanan kuvveti
ayını yönde ve aynı büyüklükte iletirler.Fakat basıncı aynen iletmezler.
|
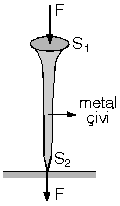
Şekildeki çivinin geniş yüzeyine
Fkuvveti uygulandığında bu kuvvet sivri uca da aynen iletilir.
Dolayısıyla sivri ucun yüzey alanı küçük olduğundan basınç daha
büyük olur.
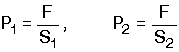
S1>>S2 olduğundan,
P2>>P1 olur.
|
 |
DURGUN SIVILARIN BASINCI
Sıvıların belli bir şekli yoktur. İçinde
bulundukları kabın şeklini alırlar. Sıvıların katılardan temel farkı
akışkan olmalarıdır. Bundan dolayı sıvılar bulundukları kabın taban
ve yan yüzeylerine yani dokundukları her noktaya basınç uygularlar.
| Ağzına kadar su dolukutunun K ve L noktalarından özdeş delik açıldığında alttaki delikten daha hızlı sıvı akışı olup daha uzaktaki bir noktaya temas eder. Bunun nedeni L noktasındaki sıvı basıncının K noktasındakinden büyük olmasıdır. Buna göre sıvı basıncı sıvı yüksekliği ile doğru orantılıdır. | 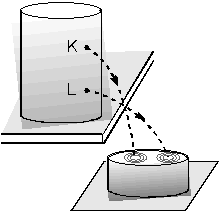 |
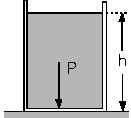
Şekilde h yüksekliğine kadar sıvı
dolu olan kabın tabanına uygulanan sıvı basıncı,
P=h.psıvı =h.d.g
bağıntısı ile hesaplanır.
|
 |
Burada, h yüksekliği, basıncın uygulandığı
noktanın sıvının açık yüzeyine olan dik yüksekliği, rsıvı
ise, sıvının özağırlığıdır.
Bu bağıntıya göre basınç hem sıvı yüksekliği,
hem de sıvının özağırlığı ile doğru orantılıdır.
Sıvı basıncı bu iki niceliğin dışında
kabın şekline ve biçimine bağlı değildir. Sıvı yüksekliği ve sıvının
özağırlığı değişmemek şartıyla sıvı hacmine de bağlı değildir.
Sıvı basıncı yüzeye daima dik olarak
etki eder. Kap yüzeyinde açılan bir delikten çıkan sıvının yüzeye dik
olarak çıkması da basıncın yüzeye dik uygulandığını gösterir.
| Şekildeki düzgün silindirik kaba akış hızı sabit olan musluktan su akıyor. Suyun yüksekliği zamanla düzgün olarak arttığı için kabın tabanındaki sıvı basıncı da zamanla düzgün olarak artar. | 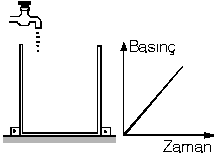 |
| Şekildeki kaba akış hızı sabit olan musluktan su akıyor. Kap yukarı doğru daraldığı için kaptaki sıvı yüksekliği zamanla daha hızlı artmaktadır. Dolayısıyla kabın tabanına etki eden sıvı basıncının artış miktarı artarak şekildeki gibi olur. | 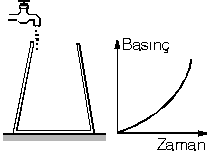 |
| Yine şekildeki kaba akış hızı sabit olan musluktan su akıyor. Kap yukarı doğru genişlediği için kaptaki sıvı yüksekliğindeki artış zamanla yavaşlayacaktır. | 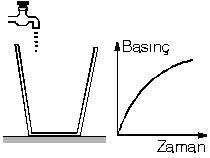 |
Dolayısıyla kabın tabanındaki sıvı basıncının
zamanla değişimi şekildeki gibi olur.
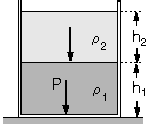
| Şekildeki kapta birbirine karışmayan
r1 ve r2 özağırlıklı sıvılar vardır. Kabın
tabanındaki toplam sıvı basıncı, sıvıların ayrı ayrı basınçlarının
toplamına eşittir.
Psıvı = h1
. r1 + h2 . r2 dir.
|
 |
BASINÇ KUVVETİ
| Bir kapta bulunan sıvı, ağırlığının etkisi ile dokunduğu bütün yüzeylere kuvvet uygular. Sıvının kap yüzeyinin tamamına uyguladığı kuvvete basınç kuvveti denir. | 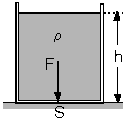 |
Şekildeki kabın taban alanı S, sıvının
özağırlığı r ve sıvı yüksekliği h ise, sıvının kap tabanına uyguladığı
basınç kuvveti
F=h.p.S bağıntısı ile hesaplanır.
| Şekildeki sıvı dolu kabın tabanına
etkiyen sıvı basınç kuvveti hesaplanırken h sıvı yüksekliği alınır.
Kabın yan yüzeylerinden birine uygulanan basınç kuvveti sorulduğunda
ise ortalama yükseklik yani |
 |
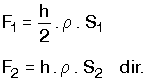
| Silindirik ve prizma şeklindeki kaplarda sıvıların kap tabanına uyguladığı basınç kuvveti sıvının ağırlığına eşittir. | 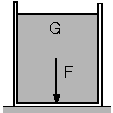 |
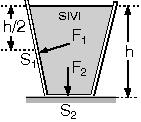
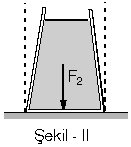
| Düşey kesiti Şekil - I deki gibi verilen kesik koni biçimindeki kabın tabanına etki eden sıvı basınç kuvveti noktalı çizgiler arasında kalan sıvının ağırlığına eşittir. Geri kalan sıvının ağırlığı yan yüzeyler tarafından dengelenir. | 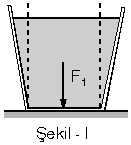 |
Şekil – II de ise yine tabana etki
e-den sıvı basınç kuvveti, noktalı çizgiler arası sıvı dolu olsaydı
o kadar sıvının ağırlığına eşit olurdu.
Buna göre, Şekil – I de basınç
kuvveti kaptaki mevcut sıvının ağırlığından küçük, Şekil – II
de ise sıvının ağırlığından büyüktür.
|
 |
SIVILARIN BASINCI İLETMESİ
(Pascal Prensibi)
İçine sıvı çekilen bir enjektörün ucu
kapatılıp piston ileri doğru itilmeye çalışıldığında, itilemediği gözlenir.
Yani sıvıların basınç altındaki hacim değişimleri önemsenmeyecek kadar
azdır. Yani pratikte sıvılar basınç altında sıkıştırılamaz.
Pascal prensibi :
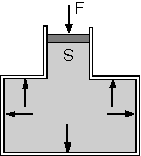
Kapalı bir kaptaki sıvının herhangi
bir noktasına uygulanan basınç kabın şekli nasıl olursa olsun,
kabın iç yüzeylerinin her noktasına sıvı tarafından aynı büyüklükte
iletilir.
Pascal prensibinden yararlanılarak,
bileşik kapların ve su cenderelerinin çalışma ilkeleri açıklanabilir.
|
 |
Bileşik Kaplar
Şekilleri ve kesitleri farklı iki
ya da daha fazla kabın tabanlarının birleştirilmesi ile elde edilen
kaplara bileşik kaplar denir. Örneğin U borusu bileşik kaptır.
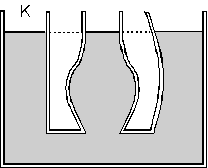
Bileşik kaplardaki sıvının üst
düzeyi hep aynı seviyededir. Örneğin kabın K kesimine bir piston
konulup sıvı aşağı doğru itilirse diğer iki koldaki sıvı eşit
miktar yükselir
|
 |
U borusunda aynı cins sıvı varken
aynı seviyedeki basınçlar eşit olur. Şekildeki U borusunda özkütleleri
farklı sıvılar varken denge sağlanmıştır. U borusunun alt kısmında
kalan sıvının özkütlesi daha büyüktür.
Yani d1 > d2
dir.
|
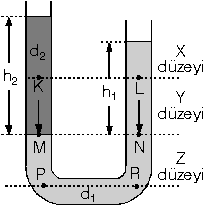 |
Alttaki sıvının en alt düzeyinden yatay çizgi çizildiğinde (Y düzeyi) bu çizgi üzerindeki basınçlar eşittir. Basınç eşitliğinden
PM = PN
h2 . d2 = h1
. d1 olur.
Z düzeyi üzerindeki P ve R noktalarındaki
basınçlar da eşittir. Fakat X düzeyi üzerindeki K ve L noktalarındaki
sıvı basınçları eşit değildir. Eğer K ve L deki basınçlar eşit olsaydı,
d1 özkütleli sıvının en üst noktası ile aynı yatay hizadaki
d2 özkütleli sıvı içindeki basınçlar da eşit olmalıydı. Bu
mümkün olmadığı için PK basıncı ile PL basıncı
da eşit olamaz, PK > PL olur.
Su Cendereleri
| Tabanları birleştirilmiş kesitleri
farklı iki silindir ve pistonlardan oluşur.
Küçük piston üzerine bir kuvvet
uygulanarak sıvı üzerine basınç uygulanır.
|
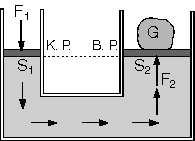 |
Pascal prensibine göre, bu basınç sıvı tarafından büyük pistona aynen iletilir. İletilen basınç büyük pistonun yüzey alanından dolayı büyük bir kuvvet oluşturur. Küçük pistona uygulanan basınç 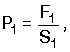 büyük pistona
uygulanan basınç P2 ise, büyük pistona
uygulanan basınç P2 ise, 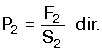
Pascal prensibine göre aynı düzeydeki
pistonların her ikisine uygulanan basınçların eşitliğinden,
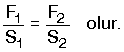
Su cendereleri basit makineye benzerler.
Kuvvetten kazanç sağlar ama yoldan da kaybettirirler.
Sıvıların basıncı iletme özelliğinden
yararlanılarak günlük hayatta kullanılan pek çok araç yapılmıştır.
Yıkama yağlama sistemlerinde arabaların kaldırılmaları, hidrolik
frenler, emme–basma tulumbaları. Bazı bitkilerin ve meyvelerin
yağını ve suyunu çıkarmada kullanılır.
|
|
AÇIK HAVA BASINCI
Dünyanın çevresindeki hava tabakası çeşitli
gazların karışımından meydana gelmiştir. Bu gaz tabakasına atmosfer
denir. Atmosferdeki gazlar da, katı ve sıvılar gibi ağırlığından dolayı
dokundukları yüzeylere basınç uygular. Bu basınca açık hava basıncı
ya da atmosfer basıncı denir.
Açık hava basıncının değeri yeryüzüne
yakın yerlerde en büyüktür. Yükseklere çıkıldıkça, hava molekülleri
azalacağı için açık hava basıncının değeri azalır.
Toriçelli Deneyi
| Yaklaşık bir metre uzunluğun da olan bir ucu kapalı cam boru alınarak ağzına kadar cıva dolduruluyor. Borunun açık kısmı el ile kapatılıp cıva çanağına daldırıldıktan sonra el çekildiğinde, cıvanın biraz çanağa boşalıp sonra sabit kaldığı görülüyor. Bu durumda borudaki cıva yüksekliği 76 cm oluyor. Borunun ağzı açık olduğu halde cıvanın tamamının çanağa boşalmamasının nedeni, cıva basıncının açık hava basıncı tarafından dengelenmesidir. | 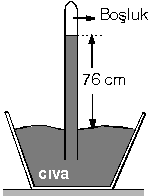 |
Aynı deney farklı genişlikteki borularla yapıldığında cıva düzeyleri arasındaki farkın yine 76 cm olduğu görülüyor. Yani borudaki cıva yüksekliği borunun kesitine bağlı değildir.
Toriçelli bu deneyi deniz seviyesinde
ve 0 °C sıcaklıkta yapmıştır.
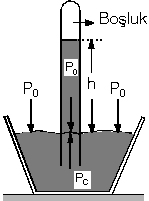
Açık hava basıncının ölçüldüğü
aletlere barometre denir. Şekildeki barometrede çanaktaki cıva
üzerine etki eden açık hava basıncı, cıva tarafından itilerek,
borudaki cıva basıncını dengeler.
Buna göre,
P0 = Pcıva
P0 = h . r = 76 . 13,6
P0 = 1033,6 g.f/cm2
dir.
Bu sonuca göre açık hava, deniz
düzeyinde 1 cm2 lik yüzeye 1 kg-f den fazla yani yaklaşık 10 N
değerinde kuvvet uygulamaktadır.
|
 |
Açık Hava Basıncının Etkileri
1.
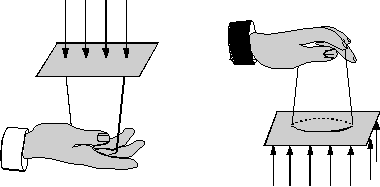

İçi su dolu bardağın ağzı hava kalmayacak
şekilde kağıtla kapatılıp şekildeki gibi ters çevrildiğinde suyun dökülmediği
görülür.
Suyun dökülmemesinin nedeni, suyun kağıda
uyguladığı basıncın, açık havanın kağıda uyguladığı basınca eşit ya
da küçük olmasıdır.
Akışkanların Basıncı
Bir yerden başka bir yere uygun şartlarda
akabilen maddelere akışkan maddeler denir. Sıvılar ve gazlar akışkan
maddelere örnektir. Akışkanlar basınç farkından dolayı akarlar ve akma
yönü basıncın büyük olduğu yerden küçük olduğu yere doğrudur.
Akışkanlarla ilgili aşağıdaki yargılar
geçerlidir.
1. Akışkanlar daima basıncın büyük olduğu
yerden küçük olduğu yöne doğru akar. Dağlarda da sular daima aşağı doğru
akar. Binaların zeminindeki strofor yardımı ile basınç farkı oluşturularak,
su binanın üst katlarına kadar çıkarılır. Odanın kapı ve penceresini
açarak hava akımı oluşturulması da basınç farkından dolayıdır.
| 2. Akışkanların kesit alanı daraldıkça akış hızı artar. Şekildeki borunun dar kesitinde akan suyun v2 hızı, geniş kesitinden akan suyun hızından büyüktür. (v2 > v1). | 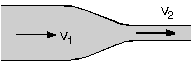 |
| Veya akışkanın hızının arttığı yerde kesit alanı daralır. Örneğin musluktan akan suyun aşağı doğru hızı artar ve kesiti daralarak incelir. | 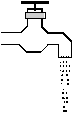 |
| 3. Akışkanın hızının arttığı yerde basıncı azalır. Şekildeki düzenekte pompa yardımıyla borunun K ucuna hava üflendiğinde, borudan sıvı yükselerek püskürür. Sıvının yükselmesinin nedeni, sıvının açık yüzeyine uygulanan açık hava basıncı L ucuna iletilir, K ucunda ise akışkanların (havanın) hızı arttığı için basınç farkı oluşur ve sıvı, basıncının büyük olduğu L ucundan, basıncın küçük olduğu K ucuna doğru hareket eder. | 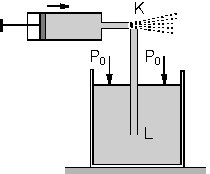 |
KAPALI KAPLARDAKİ GAZLARIN BASINCI
Gazların basıncı, gaz moleküllerinin
sürekli kabın iç çeperlerine çarpmaları sonucu oluşmaktadır. Kabın iç
yüzeyindeki birim yüzeye, birim zamanda çarpma sayısı ne kadar fazla
ise, basınç ta o kadar fazladır. Gaz moleküllerinin kabın iç yüzeyindeki
her noktaya çarpma sayısı eşit olduğundan, her noktadaki gaz basıncı
da eşit olur.
Kapalı kaptaki gazların basıncı genel
olarak üç niceliğe bağlıdır.
1. Sıcaklık ve hacim sabit ise gaz basıncı
molekül sayısı ile doğru orantılıdır. (P ~ N)
2. Sıcaklık ve molekül sayısı sabit ise,
kabın yani gazın hacmi ile ters orantılıdır. Hacim arttıkça basınç azalır,
hacim azaldıkça basınç artar.
3. Hacim ve molekül sayısı sabit ise,
gazın basıncı mutlak sıcaklıkla doğru orantılıdır. Sıcaklık arttıkça
gaz moleküllerinin hızı artar ve kabın iç yüzeyinde birim alana çarpma
sayısı artar. Bu da basıncın artmasına neden olur.
Bu üç nicelik ve basınç arasındaki ilişki
P . V = k . N . T şeklinde olur.
P ; basınç, V ; hacim, N ; molekül sayısı,
T ; mutlak sıcaklık, k ; sabit bir sayı
Boyle – Mariotte Kanunu
Bir miktar gazın sıcaklığı sabit
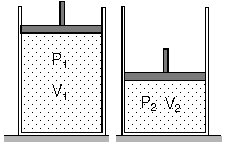
kalmak şartı ile basıncı ile hacminin çarpımı sabittir. Şekilde
piston ileri itilerek gaz sıkıştırıldığında basınç, hacim çarpımı
değişmez. P1 . V1 = P2 . V2
dir.
|
 |
Manometreler
Kapalı kaptaki gazların basınçlarını
ölçmek için kullanılan aletlere manometre denir. Manometrelerde
borunun ucu kapalı veya açık olabilir. Şekildeki cam kapta bulunan
gazın basıncı kapalı uçlu manometrede h yüksekliğindeki cıvanın
basıncına eşittir.
|
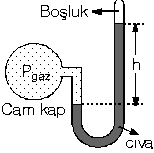 |
Pgaz = Pcıva =
h cm-Hg dir.
Bunun anlamı, gazın basıncı h yüksekliğindeki
cıvanın basıncına eşittir. Manometreler, barometrelerden faydalanılarak
yapılmıştır.
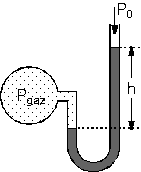
| Açık hava basıncının P0
ve cm-Hg birimi cinsinden olduğu bir ortamda, açık uçlu manometrede
cıva düzeyleri arasındaki fark şekildeki gibi h kadar ise,
Pgaz > P0
dır.
Pgaz = P0
+ h dir.
h değeri cm cinsinden ise gaz basıncı
cm-Hg cinsinden bulunur.
|
 |
Açık uçlu manometrede cıva düzeyleri
eşit ise, gazın basıncı açık hava basıncına eşittir.
Pgaz = P0 dır.
Yine açık uçlu manometrede cıva
düzeyleri arasındaki fark şekildeki gibi h kadar ise,
Pgaz < P0
dır.
Pgaz = P0
– h dir.
|
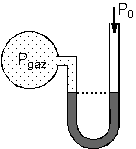 |






